반응형

1. 알켄의 친전자성 첨가 반응 복습
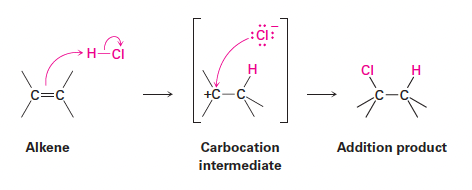
- 알켄에 HCl이 첨가될 때, 친전자성 수소가 𝛑 전자에 접근하여 한쪽 탄소와 결합함.
- 이 과정에서 카보카티온 중간체가 형성되며, 이후 친핵성 Cl- 이온과 반응하여 첨가 생성물을 형성함.
2. 방향족 고리의 반응성과 촉매의 역할
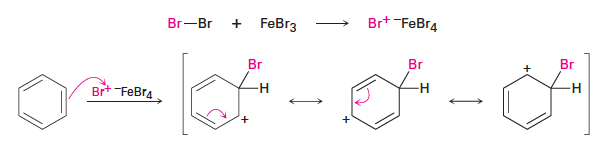
- 방향족 고리의 반응성: 알켄보다 친전자체에 대한 반응성이 낮음.
- Br2는 알켄과 즉시 반응하지만, 벤젠과는 실온에서 반응하지 않음.
- 브롬화 반응을 위해 FeBr3 촉매가 필요함.
- 촉매의 역할: Br2 분자를 편극시켜 Br+처럼 반응하는 FeBr4- Br+ 종을 생성 → 편극된 Br2가 친핵성 벤젠 고리와 반응하여 doubly allylic 성격의 비방향족 카보카티온 중간체를 형성함.
- 중간체는 3개의 공명 구조를 가져 일반 알킬 카보카티온보다 안정하지만, 150 kJ/mol의 방향족 안정성을 잃은 상태이므로 벤젠 자체보다는 훨씬 불안정함. (반응이 진행될 수 있음)
3. 알켄과 벤젠의 반응 에너지 비교
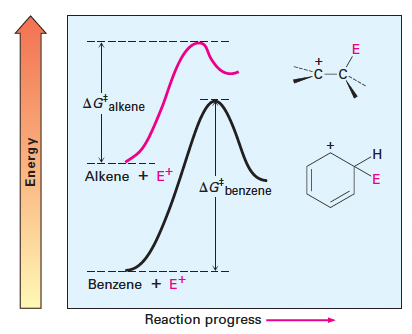
- 벤젠은 출발 물질 자체가 매우 안정하기 때문에 알켄보다 활성화 에너지(𝚫G‡)가 더 높음.
- 이로 인해 벤젠의 반응은 알켄보다 속도가 느림.
4. 브롬화 반응의 전체 메커니즘

- Step 1: 벤젠 고리의 전자쌍이 브롬을 공격하여 새로운 C-Br 결합을 만들고 비방향족 카보카티온 중간체를 형성함 (Slow).
- Step 2: 염기가 브롬이 결합한 탄소에서 H+를 제거함. C-H 결합의 전자 2개가 고리로 이동하며 방향족성을 재생함 (Fast).
- 결과적으로 H+가 Br+로 치환됨.
5. 첨가 대신 치환이 일어나는 이유

- 첨가 반응: 150 kJ/mol의 방향족 안정성을 영구적으로 상실하여 전체 반응이 흡공정(Endergonic)이 됨.
- 치환 반응: 방향족 고리의 안정성을 유지하므로 전체 반응이 발공정(Exergonic)이 됨.
Problem 16-1. Monobromination of toluene gives a mixture of three bromotoluene products. Draw and name them.
Answer.

반응형