
1. 방향족 이온의 정의와 조건
- Hückel 규칙에 따른 방향족성의 조건
- 평면 고리
- 각 원자에 p 오비탈이 있는 단일 고리 콘쥬게이션 체계
- 4n + 2개의 pi 전자를 가짐
- 이 정의는 고리 원자의 수와 pi 전자의 수가 반드시 같아야 한다거나 물질이 중성 상태여야 함을 의미하지 않으므로 중성 분자가 아닌 이온(anion 또는 cation) 형태이더라도 위 조건을 만족하면 방향족성을 가질 수 있음.
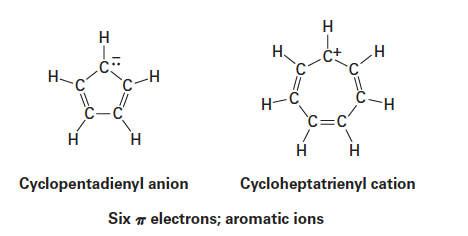
- 대표적인 예: 사이클로펜타다이에닐 음이온(Cyclopentadienyl anion), 사이클로헵타트라이에닐 양성 이온(Cycloheptatrienyl cation)
2. 방향족 이온의 형성 과정
- 수소화 이온(H:-) 제거: 결합 전자쌍을 모두 가지고 나가면 탄소 양이온(carbocation)이 생성됨.
- 수소 원자(H·) 제거: 전자 하나를 가지고 나가면 탄소 라디칼(carbon radical)이 생성됨.
- 양성자(H+) 제거: 전자쌍을 남겨두고 나가면 탄소 음이온(carbanion)이 생성됨.
- 제거 후 탄소가 sp3에서 sp2로 재혼성화되면 모든 고리 원자가 p 오비탈을 갖는 완전한 콘쥬게이션 체계가 형성됨.
- 예시: 1,3-Cyclopentadiene, 1,3,5-Cycloheptatriene

3. Hückel 규칙을 통한 안정성 예측
- 사이클로펜타다이에닐 계 (5-membered ring):
- 음이온은 6개의 pi 전자를 가져 방향족이며 매우 안정함.
- 양이온(4개)과 라디칼(5개)은 4n + 2 규칙을 만족하지 못해 불안정함.
- 사이클로헵타트라이에닐 계 (7-membered ring):
- 양이온은 6개의 pi 전자를 가져 방향족이며 매우 안정함.
- 라디칼(7개)과 음이온(8개)은 4n + 2 규칙에 어긋나 불안정하고 반방향족성을 띠기도 함.
4. 실제 화학적 성질과 안정성
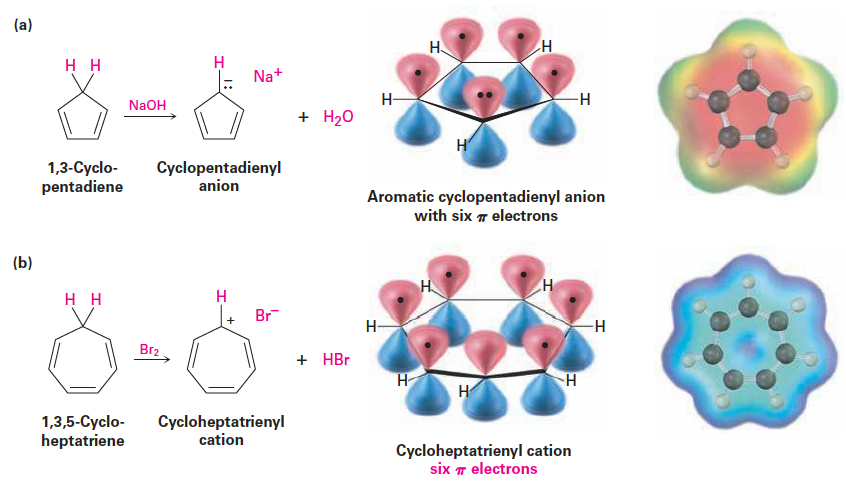
- 사이클로펜타다이에닐 음이온:
- 1,3-사이클로펜타다이엔은 pKa = 16으로, 물과 유사한 수준의 높은 산성도를 가짐.
- 이는 양성자 제거 후 형성되는 음이온이 6개의 pi 전자 방향족 체계를 형성하여 매우 안정해지기 때문임.
- 사이클로헵타트라이에닐 양이온:
- 1,3,5-사이클로헵타트라이엔에 Br2를 반응시키면 형성됨.
- 7개의 p 오비탈에 6개의 pi 전자가 비편재화되어 대칭적인 구조를 가짐.
Problem 15-6. Draw the five resonance structures of the cyclopentadienyl anion. Are all carbon–carbon bonds equivalent? How many absorption lines would you expect to see in the 1H NMR and 13C NMR spectra of the anion?
Answer.
다섯 개의 동등한 공명 구조를 그릴 수 있으며 모든 탄소-탄소 결합은 동등함. 1H NMR과 13C NMR 모두에서 각각 1개씩의 흡수선이 나타남.
Problem 15-7. Cyclooctatetraene readily reacts with potassium metal to form the stable cyclooctatetraene dianion, C8H8 2–. Why do you suppose this reaction occurs so easily? What geometry do you expect for the cyclooctatetraene dianion?
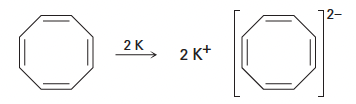
Answer.
8개의 pi 전자를 가진 중성 분자가 전자 2개를 얻어 10개의 pi 전자(4n + 2, n = 2)를 갖는 방향족 음이온이 되기 때문임. 구조는 평면 정8각형 기하 구조를 가질 것으로 예상됨.
Problem 15-8. The relative energy levels of the five pi molecular orbitals of the cyclopentadienyl system are similar to those in benzene. That is, there is a single lowest-energy MO, above which the orbitals come in degenerate pairs. Draw a diagram like that in Figure 15-5, and tell which of the five orbitals are occupied in the cation, radical, and anion.
Answer.
가장 낮은 궤도 1개와 그 위 축퇴된 궤도 2쌍이 존재함. 양이온은 낮은 에너지의 궤도 2개(3개 전자 점유), 라디칼은 3개(5개 전자 점유), 음이온은 결합성 궤도 3개(6개 전자 점유)를 채움.