반응형

1. 벤젠의 특이한 반응성

- 벤젠(C6H6)은 대응하는 육각형 고리 알칸(C6H12)보다 수소가 6개 적어 불포화 화합물로 분류되지만, 일반적인 알켄과 달리 친전자성 첨가 반응을 잘 일으키지 않음.
- 사이클로헥센은 Br2와 빠르게 반응하여 첨가 생성물을 만들지만, 벤젠은 Br2와 매우 느리게 반응하며 Fe 촉매 존재 하에서만 치환 생성물인 브로모벤젠(C6H5Br)을 형성함.
- 첨가 반응 대신 치환 반응이 일어나는 것은 벤젠의 구조적 안정성을 보여주는 중요한 증거임.
2. 수소화열을 통한 안정성 분석 (Heats of Hydrogenation)
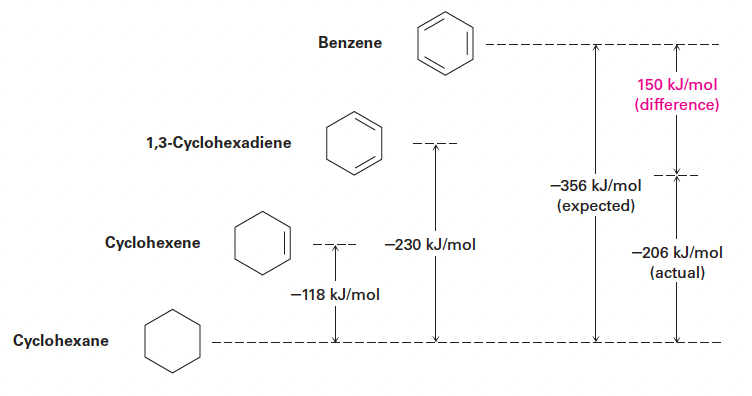
- 벤젠의 정량적인 안정성은 수소화열 측정을 통해 확인할 수 있음.
- 사이클로헥센의 수소화열: -118 kJ/mol
- 1,3-사이클로헥사다이엔(Conjugated diene)의 수소화열: -230 kJ/mol
- 세 개의 이중 결합을 가진 가상의 "사이클로헥사트라이엔"은 약 -356 kJ/mol의 수소화열을 가질 것으로 예상되나, 실제 벤젠의 측정값은 -206 kJ/mol임.
- 이 차이인 150 kJ/mol (36 kcal/mol) 만큼 벤젠은 예상보다 훨씬 낮은 에너지를 가지며, 이는 벤젠이 매우 안정하다는 것을 의미함.
3. 벤젠의 물리적 구조

- 벤젠의 모든 탄소-탄소 결합 길이: 139 pm로 동일 → 일반적인 단일 결합(154 pm)과 이중 결합(134 pm)의 중간값
- 정전기 전위 지도는 여섯 개의 모든 C-C 결합 내 전자 밀도가 동일함을 보여주며, 벤젠은 120도의 결합각을 가진 평면 정육각형 구조임.
- 모든 탄소 원자는 sp2 혼성 상태이고, 각 탄소는 고리 평면에 수직인 p 오비탈을 하나씩 가지고 있음.
4. 공명 및 분자 궤도 함수(MO)

- 공명(Resonance): 벤젠은 두 개의 동등한 공명 구조 사이의 혼성체이며, 6개의 pi 전자가 전체 고리에 걸쳐 비편재화되어 있어 안정함.
- 분자 궤도 함수(MO): 6개의 p 원자 궤도가 조합되어 6개의 벤젠 분자 궤도를 형성함.
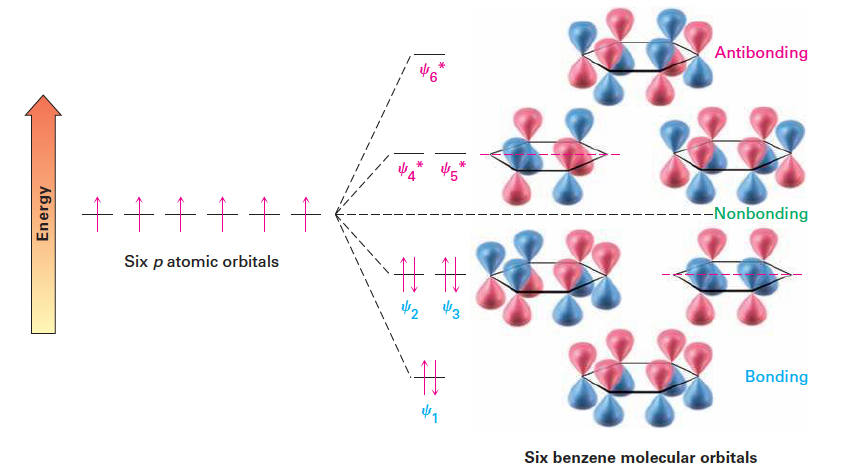
- 에너지 수준:
- 에너지가 낮은 3개의 결합성 궤도(psi 1, psi 2, psi 3)에 6개의 pi 전자가 모두 채워짐.
- 에너지가 높은 3개의 반결합성 궤도(psi 4*, psi 5*, psi 6*)는 비어 있음.
- psi 2와 psi 3, 그리고 psi 4와 psi 5는 각각 에너지가 동일한 축퇴(degenerate) 상태임.
- 이처럼 전자가 에너지가 낮은 결합성 궤도에 완전히 비편재화되어 채워지는 것이 벤젠의 특별한 안정성(150 kJ/mol)을 유발함.
Problem 15-4. Pyridine is a flat, hexagonal molecule with bond angles of 120°. It undergoes substitution rather than addition and generally behaves like benzene. Draw a picture of the pi orbitals of pyridine to explain its properties. Check your answer by looking ahead to Section 15-5.

Answer.
피리딘은 각 고리 원자(5개의 C, 1개의 N)가 평면에 수직인 p 오비탈을 가지며, 이들이 겹쳐서 벤젠과 유사한 비편재화된 pi 전자계를 형성하여 안정성을 가짐.
반응형