
1. 구조와 수소 결합
- 알코올과 페놀의 산소 원자 주위 기하 구조는 물과 유사하며, 산소 원자는 sp3 혼성 상태임.
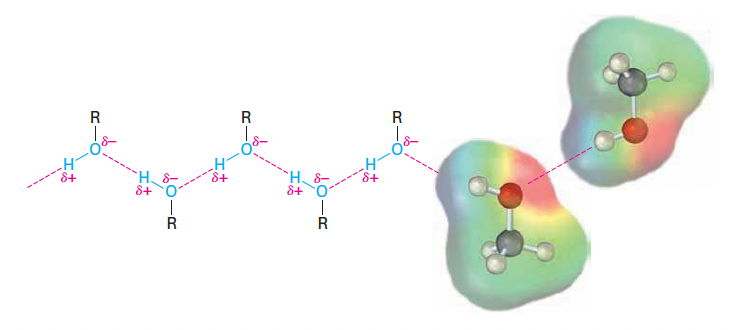
- 수소 결합(Hydrogen-bonding)으로 인해 분자 간 인력이 강하며, 비슷한 분자량의 알케인이나 할로알케인보다 끓는점이 높음.
- 예: 1-프로판올(MW=60, bp=97도), 부탄(MW=58, bp=-0.5도), 클로로에탄(MW=65, bp=12.5도).
2. 산성과 염기성
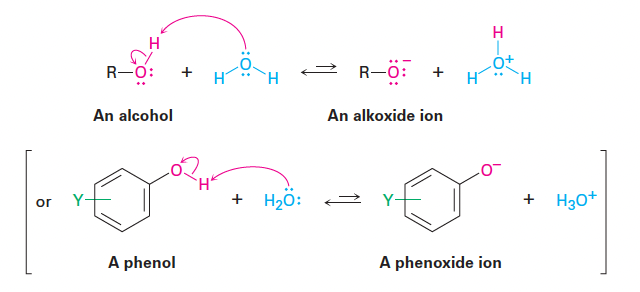
- 알코올과 페놀은 약염기이자 약산으로 작용함.
- 약염기: 강산에 의해 가역적으로 양성자화되어 옥소늄 이온(ROH2+)을 형성함.

- 약산: 묽은 수용액에서 해리되어 양성자를 내놓고 알콕사이드 이온(RO-) 또는 페녹사이드 이온(ArO-)을 형성함.
- 산성도 상수 Ka와 pKa를 통해 산의 세기를 나타내며, pKa 값이 작을수록 강한 산임.

3. 알코올의 산성도에 영향을 주는 요인
- 용매화 효과 (Solvation effects): 해리 시 생성되는 알콕사이드 이온이 물에 의해 용매화되어 안정화될수록 산성도가 높아짐.
- 메톡사이드 이온처럼 입체 장애가 적은 이온은 용매화가 쉬워 산성이 강함 (pKa=15.54).
- tert-부톡사이드 이온처럼 입체 장애가 큰 이온은 용매화가 어려워 산성이 약함 (pKa=18).

- 유도 효과 (Inductive effects): 전자 끌개 그룹(EWG)이 있으면 알콕사이드 이온의 음전하를 분산시켜 안정화하므로 산성도가 증가함.
- 예: 2,2,2-트리플루오로에탄올(pKa=12.43)은 에탄올(pKa=16)보다 훨씬 강한 산임.

4. 알콕사이드 이온의 형성
- 알코올은 매우 약한 산이므로 NaOH와 같은 약염기와는 거의 반응하지 않음.
- 알칼리 금속(Na, K) 또는 강염기(NaH, NaNH2, RMgX)와 반응하여 알콕사이드를 형성함.

5. 페놀의 산성도
- 페놀은 알코올보다 약 백만 배 더 산성이 강하며, 묽은 NaOH 수용액에 녹아 페녹사이드 염을 형성함.

- 공명 안정화 (Resonance stabilization): 페녹사이드 음이온의 음전하가 공명에 의해 벤젠 고리의 ortho, para 위치로 비편재화되어 매우 안정함.

- 치환기 효과: 전자 끌개 그룹(EWG, 예: -NO2)은 음전하를 더 비편재화시켜 산성도를 높임.
- 전자 제공 그룹(EDG, 예: -CH3)은 전하를 집중시켜 산성도를 낮춤.

Problem 17-3. The following data for isomeric four-carbon alcohols show that there is a decrease in boiling point with increasing substitution of the OH-bearing carbon. How might you account for this trend?
Answer.
알코올의 가지 수가 증가하면 면적이 좁아지고 입체 방해(steric hindrance)를 유발한다. 이는 분자 간 수소 결합을 방해하기 때문에 끓는점이 줄어든다.
Problem 17-4. Rank the following substances in order of increasing acidity:
Answer.
(a) HC≡CH < (CH3)2CHOH < CH3OH < (CF3)2CHOH
(b) p-methylphenol < phenol < p-(trifluoromethyl)phenol
(c) benzyl alcohol < phenol < p-hydroxybenzoic acid
Problem 17-5. p-Nitrobenzyl alcohol is more acidic than benzyl alcohol, but p-methoxybenzyl alcohol is less acidic. Explain.
Answer.
나이트로 기는 알콕사이드 이온을 유도 효과로 인해 안정시키는 EWG기 때문에 산도가 높다. 메톡시 기는 알콕사이드 이온을 불안정하게 하는 EDG기 때문에 산도가 낮다.