반응형

- 알켄은 극성 반응에서 친핵체(Nucleophile, Lewis base)로 작용한다.
- 탄소-탄소 이중 결합은 전자가 풍부하고, 친전자체(Electrophile, Lewis acid)에 전자쌍을 줄 수 있다.
- 알켄의 친전자성 첨가 반응 매커니즘 예시 (2-methylpropene + HBr)

- 친전자체인 HBr의 수소가 친핵성 이중 결합의 파이 전자에 의해 공격 받아 새로운 C-H 시그마 결합을 형성한다. 이때 + 전하와 비어 있는 p 오비탈을 가진 다른 탄소를 남겨두면서 탄소양이온 중간체(carbocation intermediate)를 형성한다. 동시에 H-Br 결합으로부터 두 개의 전자가 브로민으로 이동하여 브로민화 음이온(bromide ion)을 생성한다.
- 생성된 브로민화 음이온이 양전하를 띠고 있는 탄소 원자에 전자쌍을 주며 C-Br 결합을 형성하고, 전기적으로 중성인 첨가 생성물을 형성한다.
- 이러한 친전자성 첨가 반응의 에너지 도표는 탄소양이온 중간체가 생길 때 골짜기가 형성되며 두 개의 전이상태 봉우리가 되어 있다. 탄소양이온 중간체의 에너지 준위는 출발 물질인 알켄보다는 높지만 반응 전체는 자유에너지 감소 반응(exergonic)이다.

- 탄소양이온 중간체를 형성하는 첫 단계는 비교적 느리지만, 일단 생성되면 빠르게 반응하여 최종 생성물인 브로민화 알킬을 만든다.
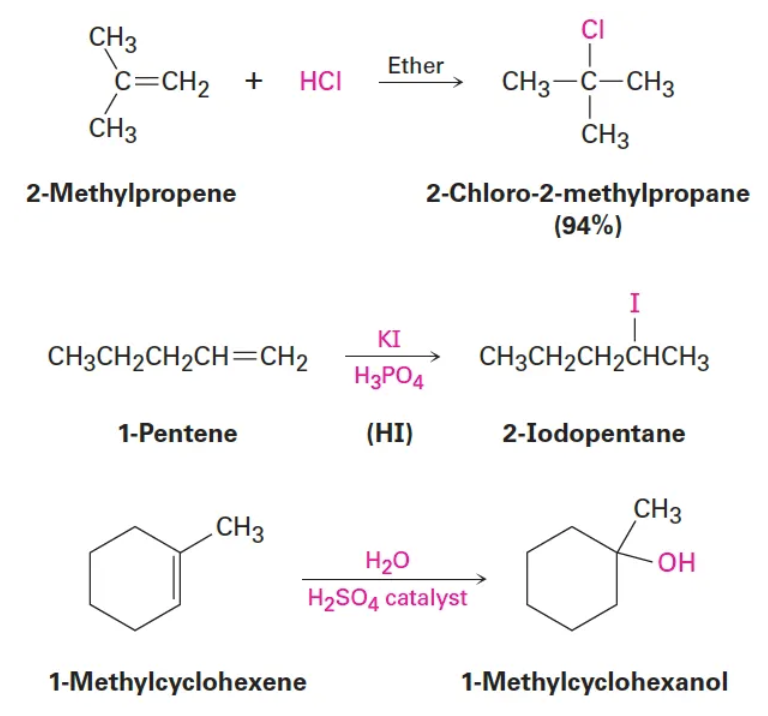
- 이러한 알켄의 친전자성 첨가 반응은 HBr 뿐만 아니라 HCl, HI, H2O 등과도 잘 일어난다.
반응형