반응형

- 유기화학에서 산화와 환원의 정의
- 유기화학에서 산화·환원은 “탄소의 전자밀도 변화”를 기준으로 정의된다.
- 산화(Oxidation): 탄소의 전자밀도 감소
- C–O, C–N, C–X 결합 형성
- C–H 결합 절단
- 환원(Reduction): 탄소의 전자밀도 증가
- C–H 결합 형성
- C–O, C–N, C–X 결합 절단
- 이 정의는 무기화학의 산화수 개념과 유사하지만, 결합의 종류를 기준으로 보다 직관적으로 판단할 수 있다.
2. 결합 변화로 판단하는 산화·환원 예시
- 탄소가 더 전기음성도가 큰 원자(O, N, halogen)와 결합할수록 산화되고, 수소와 결합할수록 환원된다.
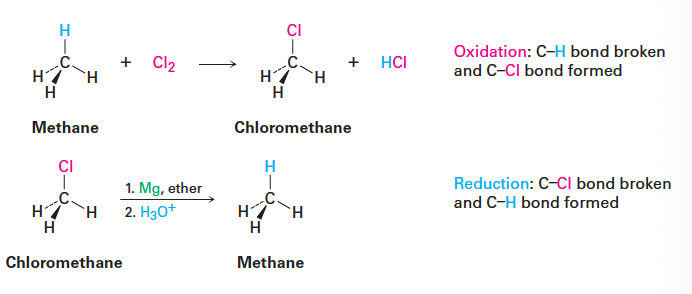
- 예시: 메탄의 염소화 반응
- C–H 결합이 끊어지고 C–Cl 결합 형성 → 산화 반응
- 예시: 알킬 클로라이드의 그리냐르 반응
- C–Cl 결합 절단, C–H 결합 형성 → 환원 반응
3. 알켄 반응에서의 산화·환원 구분
- 같은 알켄 반응이라도 시약에 따라 산화·환원 여부가 달라진다.
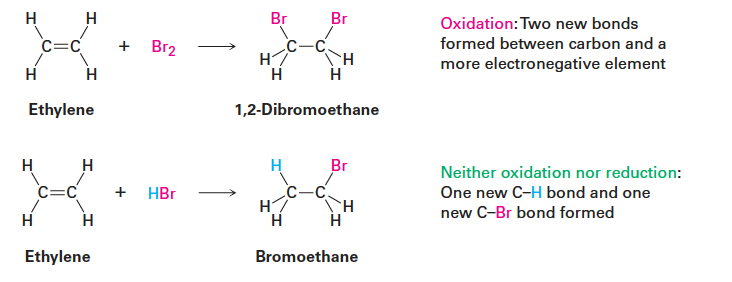
- 알켄 + Br₂ → 1,2-디브로마이드: 두 개의 C–Br 결합 형성 → 산화 반응
- 알켄 + HBr → 알킬 브로마이드: C–H 결합 1개 + C–Br 결합 1개 형성 → 산화도 환원도 아님
4. 산화 수준(oxidation level)의 개념
- 화합물은 탄소의 산화 수준에 따라 상대적으로 비교할 수 있다.
- 낮은 산화 수준 → C–H 결합이 많은 화합물 → 알케인(가장 낮음)
- 높은 산화 수준 → C–O 결합이 많은 화합물 → CO₂(가장 높음)
- 어떤 반응이
- 낮은 산화 수준 → 높은 산화 수준이면 산화 (low → high)
- 높은 산화 수준 → 낮은 산화 수준이면 환원 (high → low)
- 변화가 없으면 둘 다 아님
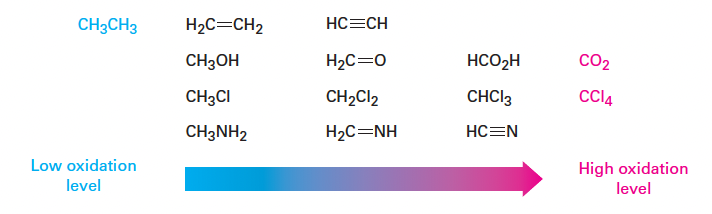
- 알케인 → 알켄 → 알카인 → 알코올/알킬 할라이드 → 알데하이드·케톤 → 카복실산 → CO₂ 순으로 갈수록 탄소의 산화 수준이 증가한다.
- 이는 C–H 결합 수 감소와 C–O, C–X 결합 수 증가로 설명된다.
산화 수준 비교 전략 (Worked Example 10-2)
- 같은 수의 탄소를 가진 화합물은 다음 기준으로 산화 수준을 비교한다.
- 전략
- (C–O + C–N + C–X 결합 수) − (C–H 결합 수)
- 값이 클수록 산화 수준이 높음
- 따라서 CH₃CH₂CH₃ < CH₃CH=CH₂ = CH₃CH(OH)CH₃ < CH₃COCH₃
Problem 10-12. Rank both sets of compounds in order of increasing oxidation level.

Answer.
(a) cyclohexane < benzene < chlorocyclohexene < cyclohexanone
(b) H₂NCH₂CH₂NH₂ < CH₃CH₂NH₂ < CH₃CN
Problem 10-13. Tell whether each of the following reactions is an oxidation, a reduction, or neither.
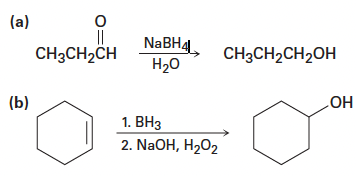
Answer.
(a) Reduction
(b) Oxidation
반응형