반응형

- 그리냐르 시약의 정의와 합성
- 그리냐르 시약(Grignard reagent): 알킬 할라이드(RX)가 마그네슘 금속과 반응하여 생성되는 유기마그네슘 화합물(RMgX)
- 그리냐르 반응은 반드시 Ether 또는 THF와 같은 비양성자성, 배위 가능한 용매에서 진행된다.
- 일반 반응식: RX + Mg → RMgX (ether or THF)
- X = Cl, Br, I
- Br, I > Cl 순으로 반응성이 높음
- 유기 플루오라이드는 거의 반응하지 않음
- 적용 가능한 기질: 1차, 2차, 3차 알킬 할라이드, 알케닐(vinylic) 할라이드, 아릴(aromatic) 할라이드
- 그리냐르 시약은 탄소–금속 결합을 포함하는 대표적인 유기금속 화합물이다.

2. C–Mg 결합의 극성과 반응성
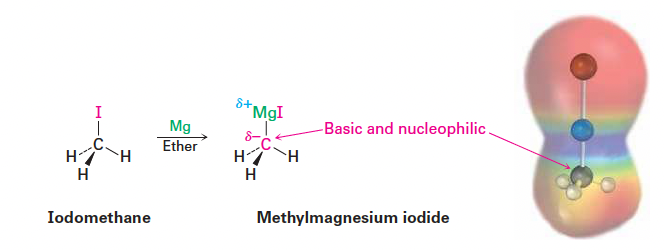
- 탄소–마그네슘 결합은 전기음성도 차이로 인해 강하게 극성화되어 있다.
- 결합 극성: C → 부분 음전하(δ⁻), Mg → 부분 양전하(δ⁺)
- 결과적 성질: 탄소는 강한 친핵체(nucleophile)인 동시에 매우 강한 염기(base)
- 따라서 그리냐르 시약은 “탄소 음이온(carbanion)의 성격”을 갖는다.
3. 그리냐르 시약의 산·염기적 성질과 안정성
- 형식적으로 그리냐르 시약은 탄소산(R₃C–H)의 마그네슘 염(R₃C⁻ MgX⁺)으로 볼 수 있다.
- 탄소산의 pKa: 약 44–60 수준 (매우 약한 산) → 그리냐르 시약은 극도로 강한 염기
- 수분 및 산에 대한 반응성
- 공기 중 수분, 알코올, 물과 즉시 반응: R–MgX + H₂O → R–H + HO–MgX
- 예시: 1-bromohexane + Mg, ether → 1-hexylmagnesium bromide + H2O → hexane 생성
- 따라서 그리냐르 반응은 반드시 무수 조건에서 수행해야 한다.
4. 합성화학에서의 역할
- 주요 특징
- 새로운 C–C 결합 형성에 활용
- 이후 챕터(Chapter 17)에서 카보닐 화합물과의 반응으로 상세히 다룸
- 개념적 중요성
- 생화학적으로 중요한 탄소 친핵체의 단순 모델 역할
Problem 10-9. How strong a base would you expect a Grignard reagent to be? Look at Table 9-1 on page 276, and predict whether the following reactions will occur as written. (The pKa of NH₃ is 35.)
(a) CH₃MgBr + H–C≡C–H → CH₄ + H–C≡C–MgBr
(b) CH₃MgBr + NH₃ → CH₄ + H₂N–MgBr
Answer.

반응은 a, b 모두 진행된다.
Problem 10-10. How might you replace a halogen substituent by a deuterium atom if you wanted to prepare a deuterated compound?
Answer.
알킬 할라이드를 Mg와 반응시켜 그리냐르 시약을 만든 뒤, D₂O로 처리하여 할로젠 위치를 중수소(D)로 치환한다.
반응형