
1. SN1 반응이 필요한 이유와 반응성 경향
- SN2 반응에 불리한 조건
- 입체 방해 (steric hinderance)가 매우 큰 기질
- 중성 친핵체
- protic solvent
- 3차 알킬 할라이드 + H₂O 반응은 매우 빠름 → SN2 반응이 아닌 다른 메커니즘
- 예시: (CH₃)₃CBr + H₂O → (CH₃)₃COH + HBr
- CH₃Br + H₂O 반응보다 10⁶배 이상 빠름
- 실험적 반응성 순서 (SN1): SN2와 정반대 경향

2. SN1 반응의 속도론적 특징
- SN1 = Substitution, Nucleophilic, Unimolecular
- 반응 속도는 알킬 할라이드 농도에만 의존
- 속도식: Reaction rate = k[RX]
- 친핵체 농도는 속도식에 포함되지 않음
- 속도결정단계 (RDS, Rate Determining Step): 다단계 반응에서 가장 높은 ΔG‡를 갖는 단계
- SN1 반응에서는 알킬 할라이드의 자발적 해리 → 카보양이온 형성 ⇒ 이 단계가 가장 느리므로 속도결정단계
3. SN1 반응 메커니즘 (3단계)
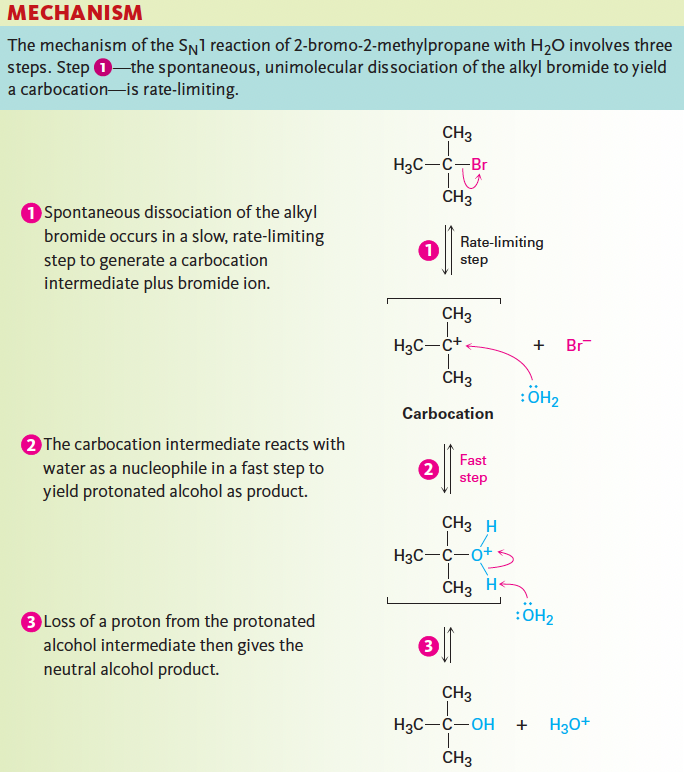
- Step 1 (느림, 속도결정단계): RX → R⁺ + X⁻ (알킬 할라이드가 해리되어 카보양이온 생성)
- Step 2 (빠름): 카보양이온 + 친핵체(H₂O) → 양성자화된 알코올
- Step 3 (빠름): 탈양성자 → 중성 알코올 생성
- 핵심 특징
- 친핵체는 속도결정단계에 관여하지 않음
- leaving group이 먼저 떨어짐
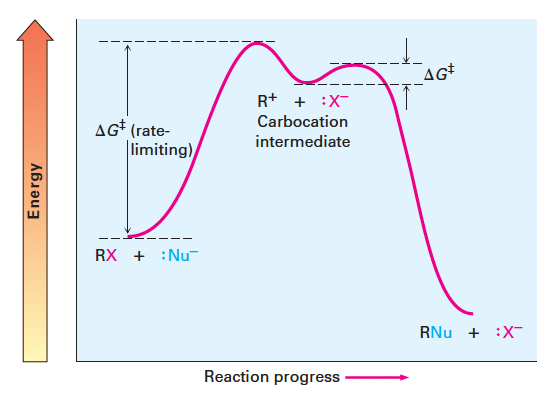
- SN1 반응의 에너지 다이어그램: 두 개의 전이상태 존재
- 첫 번째 봉우리: RX 해리 (가장 큼, rate-limiting)
- 두 번째 봉우리: 친핵체 결합
- 카보양이온 중간체가 안정할수록 반응 빠름
4. 입체화학: 라세미화 경향
- SN1 반응은 카보양이온 중간체를 거침
- 카보양이온: sp² 혼성, 평면 구조, achiral → 친핵체가 양쪽에서 공격 가능
- 50% inversion + 50% retention → 라세미 혼합물
- 실제 SN1 반응에서의 불완전한 라세미화: 실험적으로는 완전한 라세미화가 드묾
- 일반적으로 inversion이 약간 우세 (0–20% excess)
- 원인: ion pair 효과
- 떠난 X⁻가 카보양이온 한쪽 면을 부분적으로 차폐
- 완전한 자유 카보양이온 형성 전 치환 발생 가능
- 결과: 한쪽 면 공격이 상대적으로 유리 → 부분적 inversion 우세

Problem 11-8. What product(s) would you expect from reaction of (S)-3-chloro-3-methyloctane with acetic acid? Show the stereochemistry of both reactant and product.
Answer.
SN1 반응 → 카보양이온 중간체 형성 → 아세테이트에 의해 치환
→ 주생성물: 3-acetoxy-3-methyloctane
→ 입체화학: 라세미 혼합물 (inversion + retention)
Problem 11-9. Among the many examples of SN1 reactions that occur with incomplete racemization, the optically pure tosylate of 2,2-dimethyl-1-phenyl-1-propanol ([a]D 5 230.3) gives the corresponding acetate ([a]D 5 15.3) when heated in acetic acid. If complete inversion had occurred, the optically pure acetate would have had [a]D 5 153.6. What percentage racemization and what percentage inversion has occurred in this reaction?
Answer.
관측 회전값 / 완전 inversion 회전값 = 5.3 / 53.6 ≈ 0.10 → 약 10% inversion → 약 90% racemization
Problem 11-10. Assign configuration to the following substrate, and show the stereochemistry and identity of the product obtained by SN1 reaction with water.
Answer.
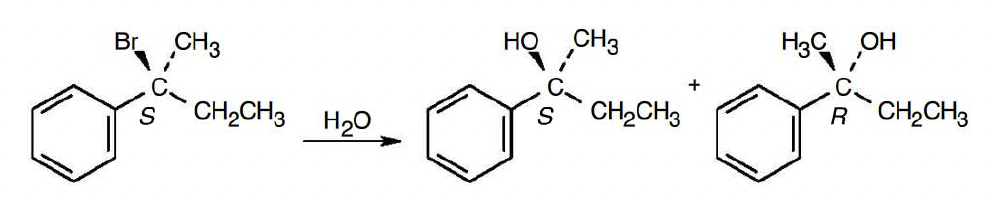
50:50 비율로 enantiomer 생성
'전공필수 > 유기화학 (Organic chemistry)' 카테고리의 다른 글
| [유기화학] 11-6. 생물학적 치환 반응 (Biological Substitution Reactions) (0) | 2026.01.08 |
|---|---|
| [유기화학] 11-5. SN1 반응의 특징 (Characteristics of the SN1 Reaction) (0) | 2026.01.07 |
| [유기화학] 11-3. SN2 반응의 특성 (Characteristics of the SN2 Reaction) (0) | 2026.01.05 |
| [유기화학] 11-2. SN2 반응 (The SN2 Reaction) (0) | 2026.01.04 |
| [유기화학] 11-1. 친핵성 치환 반응의 발견 (The Discovery of Nucleophilic Substitution Reactions) (0) | 2026.01.03 |