
1. 반응의 기본 개념
- 알켄에 Br₂ 또는 Cl₂가 첨가되면 항상 1,2-dihalide가 형성된다.
- 예: Ethylene + Cl₂ → 1,2-dichloroethane
✔ 반응성 순서
- F₂ : 지나치게 반응성이 커 실험적 적용 어려움
- Br₂, Cl₂ : 할로젠화 반응에서 주로 사용
- I₂ : 대부분의 알켄과는 반응하지 않음 (열역학적으로 불리)
2. 단순한 카보양이온 메커니즘의 문제점
- 처음 떠올릴 수 있는 메커니즘: Br₂의 Br⁺가 알켄에 친전자성 첨가 → 카보양이온 형성 → Br⁻가 공격 → dibromide 생성
- 하지만 이 메커니즘은 입체화학(stereochemistry)을 설명하지 못한다.
- 평면 카보양이온이 중간체라면 → cis/trans 이성질체 모두 나와야 하기 때문.
3. 실제 반응의 입체화학성: anti stereochemistry
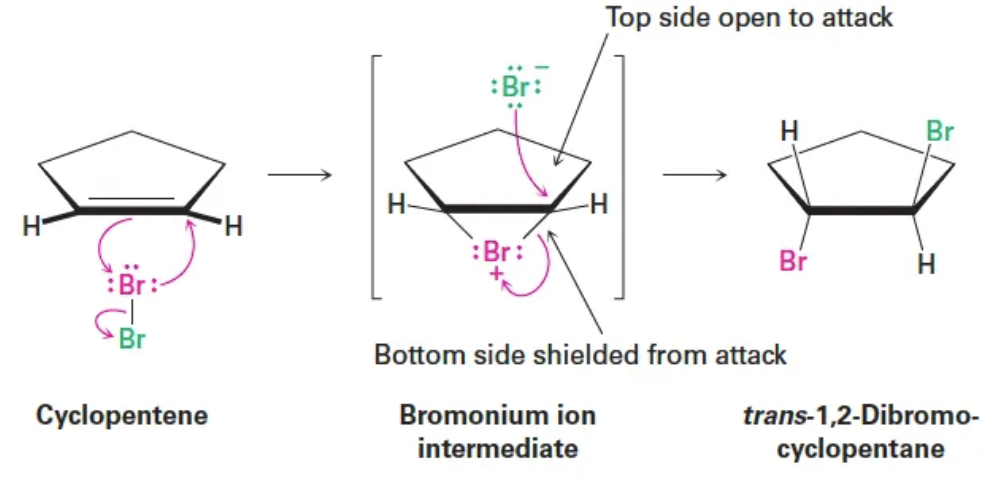
- Cyclopentene에 Br₂를 첨가하면 trans-1,2-dibromocyclopentane만 생성 (sole product)되며, cis-1,2-dibromide는 전혀 생성되지 않음.
- 이는 반응이 anti addition임을 의미한다. 즉, 두 Br 원자는 이중결합의 반대 면에서 각각 등장한다.
- 이 결과는 카보양이온 중간체로는 설명 불가.

4. 브로모늄 이온 중간체 (Bromonium ion)
- 1937년 Kimball & Roberts가 제안한 올바른 메커니즘: 브로모늄 이온 (bromonium ion) 형성
- Br₂가 알켄에 접근 → π 전자가 Br에 공격 → 동시에 Br–Br가 끊어지며 Br⁻가 빠져나감 → 남은 Br⁺가 두 탄소에 동시에 결합하여 3원환 양전하 중간체(bromonium ion) 형성

- 이후 backside attack: 브로모늄 이온의 한쪽 면이 Br⁺에 의해 막혀 있기 때문에, Br⁻는 반대쪽(backside)에서만 공격할 수 있다. → 이 때문에 anti-addition이 발생.
5. cycloalkene에서 anti가 잘 드러나는 이유
- Cyclopentene의 경우, 브로모늄 이온이 형성되면 Br⁺가 한쪽 면을 완전히 가린다(steric blocking)
- 따라서 복면(반대쪽 face)만 공격 가능 → 항상 trans-1,2-dibromide 생성, cis 생성물 없음
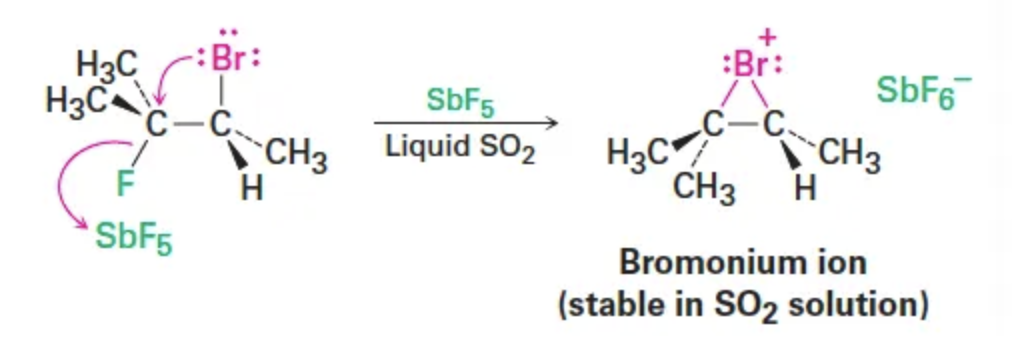
6. 브로모늄/클로로늄 이온의 실제 존재 증거: George Olah는 실제로 cyclic bromonium ions를 액체 SO₂(SbF₅와 함께)에서 안정적으로 분리·관찰함 → 브로모늄/클로로늄 이온이 단순한 가설이 아니라 실제 존재하는 중간체임을 강하게 뒷받침.
7. 생체 내 할로젠화 (Haloperoxidases)
- 생물학적으로도 할로젠화 반응이 존재하는데, 해양 생물의 haloperoxidase 효소가 다음을 수행한다.
- H₂O₂를 이용하여 Br⁻, Cl⁻를 산화 → Br⁺, Cl⁺ equivalent 생성 → 알켄과 반응 → 브로모늄/클로로늄 이온 형성 → 할라이드와 추가 반응 → 다할로겐화된 생리활성 물질 생성
- 예: red algae에서 발견된 Halomon (5개 할로겐 포함)
Problem 8-3. What product would you expect to obtain from addition of Cl2 to 1,2-dimethylcyclohexene? Show the stereochemistry of the product.
Answer.
trans-1,2-dichloro-1,2-dimethylcyclohexane
Problem 8-4. Addition of HCl to 1,2-dimethylcyclohexene yields a mixture of two products. Show the stereochemistry of each, and explain why a mixture is formed.
Answer.
HCl 첨가는 브로모늄 이온이 아닌 카보양이온 매커니즘으로 재배열 가능성이 있음. 따라서 혼합물로 생성됨.