
1. 치환기가 반응 속도 및 위치에 미치는 영향
- 치환된 벤젠 고리에 새로운 친전자체가 들어올 때, 기존의 치환기는 반응의 속도와 위치에 두 가지 영향을 미침.
- 반응성(Reactivity)에 미치는 영향
- 활성제 (Activators): 벤젠보다 반응 속도를 빠르게 함. (예: -OH기는 벤젠보다 약 1000배 더 반응성이 큼.)
- 비활성제 (Deactivators): 벤젠보다 반응 속도를 느리게 함. (예: -NO2기는 벤젠보다 약 1000만 배 이상 반응성이 낮음.)
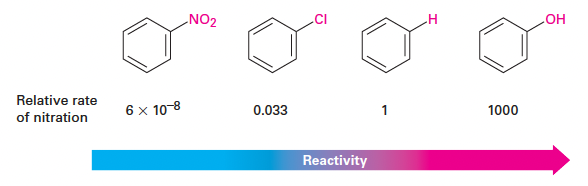
- 배향성(Orientation)에 미치는 영향
- Ortho 및 Para 지향기: 새로운 치환기가 주로 ortho(1,2-위치)나 para(1,4-위치)에 결합하도록 유도함.
- Meta 지향기: 새로운 치환기가 주로 meta(1,3-위치)에 결합하도록 유도함.

2. 치환기의 분류 (Table 16-1) ⭐️⭐️⭐️⭐️⭐️
- Ortho- 및 Para-지향 Activator: -NH2, -OH, -NHCOCH3, -OCH3, 알킬기(-CH3 등).
- Ortho- 및 Para-지향 Deactivator: 할로젠 원소(-F, -Cl, -Br, -I). 반응성은 낮추지만 배향성은 ortho, para로 유도함.
- Meta-지향 Deactivator: -CHO, -COCH3, -CO2CH3, -CO2H, -CN, -NO2, -NR3+. (강력하게 반응성을 낮춤.)

3. 활성 및 비활성 효과 (Activating and Deactivating Effects)
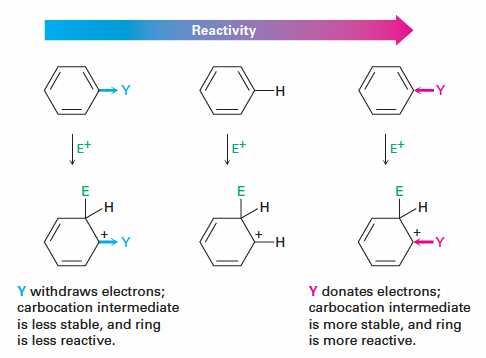
- 활성기(Activating group)
- 고리에 전자를 제공하여 전자 풍부(electron-rich) 상태로 만듦.
- 탄소 양이온 중간체를 안정화하여 활성화 에너지를 낮춤.
- 비활성기(Deactivating group)
- 고리로부터 전자를 끌어당겨 전자 부족(electron-poor) 상태로 만듦.
- 탄소 양이온 중간체를 불안정하게 하여 활성화 에너지를 높임.
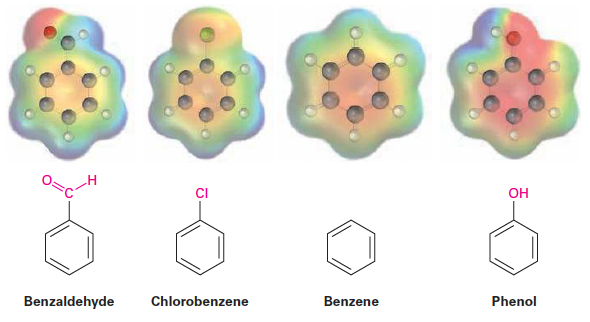
- 정전기 전위 지도
- Electron-withdrawing group (EWG; -CHO, -Cl): 고리를 더 양전하(황녹색)로 만듦.
- Electron-donating group(EDG, -OH): 고리를 더 음전하(빨간색)로 만듦.
- 유도 효과 (Inductive Effects)
- 유도 전자 흡인(Inductive electron withdrawal): 전기 음성도 차이로 인해 sigma(σ) 결합을 통해 전자를 끌어당김. 할로젠, 하이드록실, 카보닐, 사이아노, 니트로기 등이 이에 해당함.
- 유도 전자 공여(Inductive electron donation): 알킬기는 초공액(hyperconjugation)을 통해 고리에 전자를 제공함.

- 공명 효과 (Resonance Effects)
- 공명 전자 흡인(Resonance electron withdrawal): 치환기가 p 오비탈 중첩을 통해 고리의 π 전자를 끌어당김. -Y=Z 형태(Z가 더 전기음성적)인 카보닐, 사이아노, 니트로기가 해당함.
- 공명 전자 공여(Resonance electron donation): 비공유 전자쌍을 가진 치환기가 π 결합을 통해 고리에 전자를 제공함. 할로젠, 하이드록실, 알콕실(-OR), 아미노(-NH2) 기가 해당함.

- 효과의 상충과 Net effect: 한 치환기의 유도 효과와 공명 효과가 상충될 경우
- 활성제 (-OH, -NH2 등): 강한 공명 전자 공여 효과가 약한 유도 전자 흡인 효과를 압도하여 고리를 활성화함.
- 비활성제 (할로젠): 강한 유도 전자 흡인 효과가 약한 공명 전자 공여 효과보다 우세하여 고리를 비활성화함.
4. Ortho- 및 Para-지향 활성제: 알킬기 (Alkyl Groups)
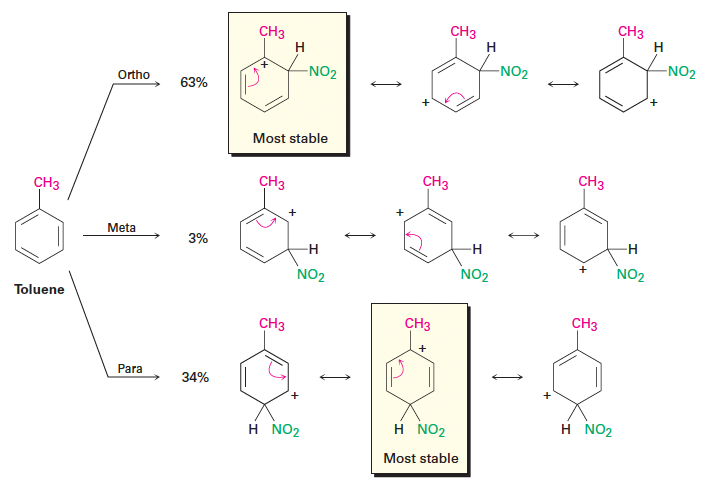
- ortho 및 para 위치: 생성되는 탄소 양이온 중간체는 양전하가 알킬기가 붙은 3차 탄소에 위치하여 매우 안정함.
- meta 위치: 양전하가 2차 탄소에만 머무르므로 ortho/para 중간체보다 불안정하여 반응이 거의 일어나지 않음.
5. Ortho- 및 Para-지향 활성제: -OH 및 -NH2
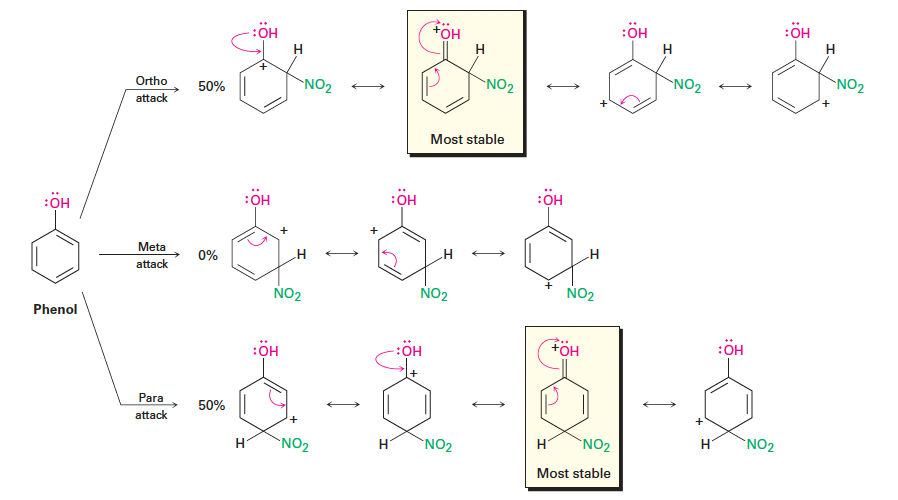
- 강력한 공명 전자 공여를 통해 ortho 및 para 중간체를 안정화함.
- 양전하가 치환기가 붙은 탄소에 올 때, 산소나 질소의 비공유 전자쌍이 추가적인 공명 구조를 형성하여 안정성을 크게 높임.
6. Ortho- 및 Para-지향 비활성제: 할로젠 (Halogens)

- 할로젠은 고리를 비활성화시키지만, ortho 및 para 공격 시에는 비공유 전자쌍을 통해 양전하를 안정화하는 공명 구조를 가짐.
- meta 중간체는 이러한 공명 안정화가 불가능하므로 ortho 및 para 생성물이 주로 형성됨.
7. Meta-지향 비활성제 (Meta-Directing Deactivators)
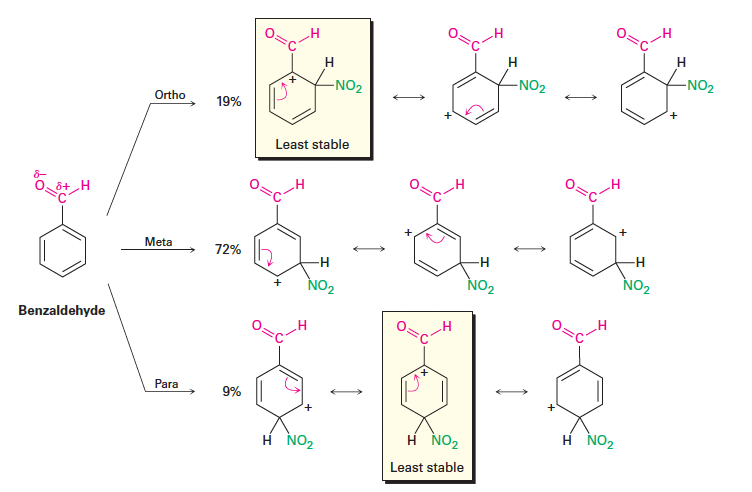
- ortho 및 para 위치:카보닐기(-CHO)와 같이 양전하를 띤(δ+) 원자가 고리에 직접 붙은 경우, ortho 및 para 공격 시 양전하가 서로 인접하는 매우 불안정한 공명 구조가 형성됨.
- meta 위치: meta 중간체는 양전하가 서로 멀리 떨어져 있어 상대적으로 더 선호되며 반응이 더 빠름.
8. 친전자성 방향족 치환반응의 치환기 효과 요약 ⭐️⭐️⭐️⭐️⭐️
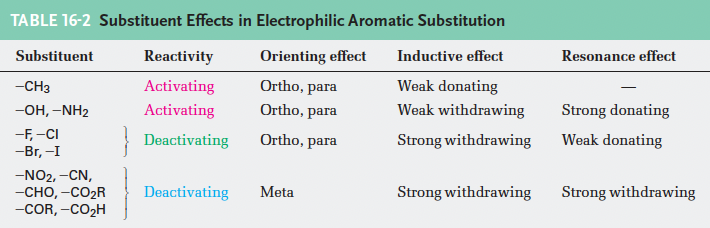
Problem 16-8. Rank the compounds in each of the following groups in order of their reactivity to electrophilic substitution:
(a) Nitrobenzene, phenol, toluene, benzene
(b) Phenol, benzene, chlorobenzene, benzoic acid
(c) Benzene, bromobenzene, benzaldehyde, aniline
Answer.
(a) Phenol > Toluene > Benzene > Nitrobenzene
(b) Phenol > Benzene > Chlorobenzene > Benzoic acid
(c) Aniline > Benzene > Bromobenzene > Benzaldehyde
Problem 16-9. Predict the major products of the following reactions:
(a) Nitration of bromobenzene (b) Bromination of nitrobenzene
(c) Chlorination of phenol (d) Bromination of aniline
Answer.
(a) o-Bromonitrobenzene + p-Bromonitrobenzene
(b) m-Bromonitrobenzene
(c) o-Chlorophenol + p-Chlorophenol
(d) o-Bromoaniline + p-Bromoaniline
Problem 16-10. Use Figure 16-11 to explain why Friedel–Crafts alkylations often give polysubstitution but Friedel–Crafts acylations do not.

Answer.
알킬기는 고리를 더 반응성있게 만들어 추가적인 치환이 일어나게 만드는 활성화기다. 반면 아실기는 고리를 덜 반응성있게 만들어서 추가적인 치환을 막는 비활성기다.
Problem 16-11. An electrostatic potential map of (trifluoromethyl)benzene, C6H5CF3, is shown. Would you expect (trifluoromethyl)benzene to be more reactive or less reactive than toluene toward electrophilic substitution? Explain.

Answer.
Less reactive. 음전하를 지닌 3개의 F 원자가 유도 효과로 강하게 전자를 고리로부터 끌어당기므로, 고리를 더 전자가 부족하고 deactivating하기 때문이다. 반면 톨루엔의 메틸기는 electron-donating group (EDG)로 반응성을 더 좋게 한다.
Problem 16-12. Acetanilide is less reactive than aniline toward electrophilic substitution. Explain.

Answer.
아민의 비공유전자쌍이 공명 효과에 의해 인접한 카보닐기에 delocalized되어 있어 벤젠 고리로 전자를 줄 수 없기 때문이다.
Problem 16-13. Draw resonance structures for the intermediates from the reaction of an electrophile at the ortho, meta, and para positions of nitrobenzene. Which intermediates are most stable?
Answer.

Meta가 가장 stable.